ESGO 2009 - HPV-Impfung: Update 2009
In Belgrad hat vom 11. bis 14. Oktober 2009 das 18th International Meeting of the European Society of Gynaecologycal Oncology stattgefunden. Dieser Bericht fasst das aktuelle Wissen rund um die Zervixkarzinomprophylaxe durch die quadrivalente HPV-Impfung zusammen.
 |
|
ESGO 2009 - Belgrad | |
|
Präsentationen von X. Castellsagué, Barcelona (Spanien); E.A. Joura, Wien (Österreich); M. Poljak, Ljubljana (Slowenien); A. Saah, North Wales (USA); O.E. Iversen, Bergen (Norwegen); C. Sattler, West Point (USA)
HPV-Problematik bei erwachsenen Frauen
Bei den 15-44-jährigen Frauen ist das Zervixkarzinom nach Brustkrebs der zweithäufigste maligne Tumor in Europa und derjenige mit der zweithöchsten Mortalität. In einzelnen Ländern beispielsweise Serbien, dem Gastgeberland des ESGO 2009 unterscheidet sich die Inzidenz und Mortalität kaum von den entsprechenden Zahlen für Brustkrebs [1].
Jedes Jahr treten bei Frauen ungefähr 530'000 neue durch HPV verursachte Malignome auf. Beim Zervixkarzinom sind 95-98%, beim Vulvakarzinom 30-35%, beim Vaginalkarzinom 65-90% und beim Analkarzinom über 80% der Fälle HPV-assoziiert. In den letzten Jahren zeigte sich auch, dass in bis zu einem Drittel der oropharyngealen Tumore HPV nachweisbar ist. Die mit Abstand am häufigsten nachgewiesenen Typen sind auch bei den Nicht-Zervixkarzinomen HPV-16 und -18, in Vulvakarzinomen ca. 80%, in Analkarzinomen sogar über 90%. HPV scheint damit nach Tabak das zweitwichtigste humane Karzinogen zu sein.
Das durch HPV verursachte Leiden geht aber über die Malignome hinaus. Die HPV-Typen 6 und 11 sind zu einem beträchtlichen Anteil an der Entstehung von genitalen Warzen beteiligt. HPV-6, -11, -16 und -18 finden sich in bis zu 84% der genitalen Warzen. Kondylome haben bei Frauen sowie bei Männern in den letzten 30 Jahren um ein Vielfaches zugenommen.
HPV nicht nur in der Adoleszenz ein wichtiges Pathogen
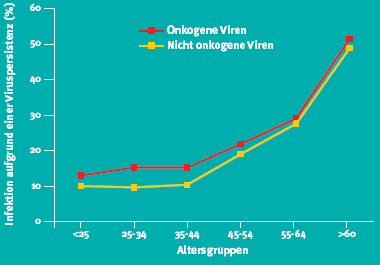
Die Kurve der HPV-Prävalenz sinkt bei über 25-jährigen Frauen weltweit während einigen Jahren ab, um dann aber zwischen 35 und 45 Jahren wieder anzusteigen [2]. Dies gilt auch ganz spezifisch für die onkogenen Viren [3]. Das kumulative Risiko einer Frau, im Leben mit HPV infiziert zu werden, steigt mit jedem Jahr an; und damit erhöht sich auch das Risiko für eine HPV-Persistenz stetig (siehe Abbildung 1) [4]. Khan und Kollegen konnten denn auch nachweisen, dass das kumulative Progressionsrisiko von einer HPV-16 oder -18 Infektion in eine CIN3+-Läsion über die Jahre zunimmt [5]. Zusätzlich werden bis im Alter von 50 Jahren neu 1-2 Kondylome pro 1000 Frauenjahre diagnostiziert [6].
 |
|
Abbildung 1: Risiko einer HPV-Persistenz je nach Alter | |
| |
Die Schlussfolgerung von Prof. Castellsagué sinngemäss: Das Risiko für HPV-assoziierte Erkrankungen beginnt mit den ersten sexuellen Erfahrungen und bleibt lebenslang bestehen. Obwohl neue Infektionen mit dem Alter weniger häufig auftreten, nimmt das Persistenzrisiko zu. Diese Erkenntnisse zeigen, wie wichtig die HPV-Protektion durch die quadrivalente Impfung auch im Alter zwischen 25 und 45 Jahren ist.
Neue Daten zur Effektivität und Sicherheit der quadrivalenten HPV-Impfung
Die quadrivalente HPV-Impfung hat sich zur Prävention von zervikalen intraepithelialen Neoplasien bei jungen Frauen als hoch effektiv erwiesen [7]. Gemäss einer am ESGO 2009 präsentierten Analyse von über 17'000 geimpften, initial HPV-naiven Frauen mit einem Follow-up von bis zu 4 Jahren konnten CIN 1-3 und AIS (Adenocarzinoma in situ) um 94% reduziert werden [8]. Der Schutz gegen Erkrankungen mit in der Impfung abgedeckten HPV-Typen lag zwischen 95% und 100%. Eine Langzeitbeobachtung zeigte, dass die klinische Effektivität der Impfung gegen HPV-16 über einen Zeitraum von 9.5 Jahren bei 100% erhalten bleibt [9].
Neben der Protektion gegen HPV-6, -11, -16 und -18 besteht auch ein gewisser Kreuz-Schutz gegen andere HPV-Typen durch die quadrivalente Impfung, wie neuste Analysen zeigen [10]. Die Effektivität gegen CIN2, CIN3 oder AIS lag je nach HPV-Typ zwischen 33% und 70%.
Reduktion extrazervikaler Erkrankungen bis ins Alter von 45
Im New England Journal of Medicine und im Lancet publizierte Studien haben 2007 gezeigt, dass die quadrivalente Impfung auch vulväre und vaginale intraepitheliale Neoplasien verhindern kann, den Untersuchungen zufolge mit einem 100%igen Schutzfaktor [11,12]. Kürzlich konnten Harper und Kollegen ausserdem nachweisen, dass genitale Warzen bei geimpften Frauen zwischen 16 und 45 Jahren signifikant seltener auftraten als bei nicht geimpften [13]. Dabei betrug die Protektionsrate bei den 24- bis 45-jährigen Frauen für genitale Erkrankungen, die durch HPV-6, 11, 16 oder 18 bedingt waren, 92% [14].
Auch vorbehandelte Frauen profitieren
Frauen, welche bereits eine Therapie einer HPV-assoziierten Erkrankung über sich ergehen lassen mussten, haben ein speziell hohes Risiko für die Entwicklung einer zervikalen intraepithelialen Neoplaise (CIN). Nach einer Behandlung einer zervikalen Läsion ist das Risiko etwa um den Faktor 3 erhöht, nach Behandlung von genitalen Warzen, einer vulvären oder einer vaginalen intraepithelialen Neoplaise sogar um den Faktor 10. Bisher war nicht bekannt, ob diese Population von der HPV-Impfung profitiert oder nicht.
Prof. Joura hat am ESGO 2009 eine Analyse von 587 Frauen aus dem Impfungsarm und 763 Frauen aus dem Placeboarm der FUTURE I und II Studien präsentiert [15]. Diese Studienteilnehmerinnen mussten sich aufgrund kolposkopischer und histologischer Befunde einer zervikalen Therapie unterziehen (in den meisten Fällen einer Konisation). Endpunkt der Studie war der Einfluss der quadrivalenten HPV-Impfung auf die Entwicklung neuer CIN, genitaler Warzen und vulvärer sowie vaginaler intraepithelialer Neoplasien.
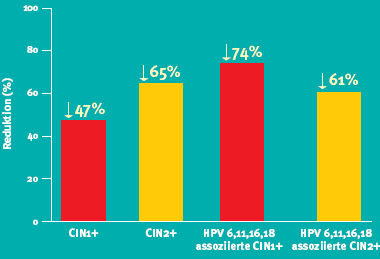
Die Inzidenz neuer zervikaler intraepithelialer Läsionen nach Vorbehandlung einer solchen konnte durch die Impfung stark gesenkt werden, wie Abbildung 2 illustriert. Aber nicht nur zervikale, sondern auch genitale Warzen sowie vulväre und vaginale HPV-assoziierte Neuerkrankungen wurden um 46% reduziert; HPV-6, -11, -16 oder -18 assoziierte Läsionen sogar um 82%. Ähnliche Resultate zeigte die Analyse bei Frauen mit einer Vorbehandlung von genitalen Warzen, vulvären oder vaginalen intraepithelialen Neoplasien. Diese Studienergebnisse zeigen zum ersten Mal, dass auch wegen HPV-assoziierten Erkrankungen vorbehandelte Frauen von der quadrivalenten Impfung profitieren.
 |
|
Abbildung 2: Reduktion von CIN bei vorbehandelten Frauen | |
| |
Impfung auch nach HPV-Exposition wirksam
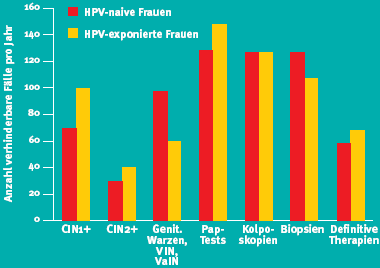
Interessant sind die Ergebnisse von zwei am ESGO 2009 vorgestellten Studien, welche den Einfluss der quadrivalenten Impfung auf die Inzidenz von Erkrankungen durch irgend einen HPV-Typen untersuchten ,und zwar bei HPV-naiven und HPV-exponierten Frauen [16,17]. Die Autoren beobachteten bei den geimpften Frauen gegenüber der Placebogruppe eine beträchtliche Reduktion von zervikalen, vulvären und vaginalen intraepithelialen Neoplasien sowie von Pap-Tests und Interventionen - bei den bei Impfung HPV-naiven und bereits HPV-exponierten Frauen. Eine Übersicht über die zu erwartende Anzahl verhinderbarer Fälle durch die Impfung gibt Abbildung 3:
 |
|
Abbildung 3: Fälle pro 10'000 Frauen, welche durch die Impfung zu verhindern wären | |
| |
HPV-Impfung bei Männern: Erste Ergebnisse
Bei Männern besteht durch die Infektion mit HPV ein erhöhtes Risiko für genitale Warzen
- Rezidivierende respiratorische Papillomatose
- Analkarzinome
- Oropharyngeale Karzinome
- Peniskarzinome
Ausserdem spielt der Mann eine grosse Rolle als Transmitter von HPV auf Frauen, welche allenfalls nicht geimpft sind.
Erste Resultate einer Studie an 2'800 16- bis 23-jährigen Männern sprechen für eine viel versprechende Wirksamkeit der quadrivalenten Impfung nicht nur bei Frauen. Der Schutz vor externen genitalen Läsionen betrug gemäss Prof. Joura nach einem Follow-up von durchschnittlich 3 Jahren 90%, bei der Berücksichtigung lediglich der durch die onkogenen HPV-Typen 16 und 18 verursachten Läsionen sogar 100% [18].
Real-life Daten zeigen das Potenzial der Impfung
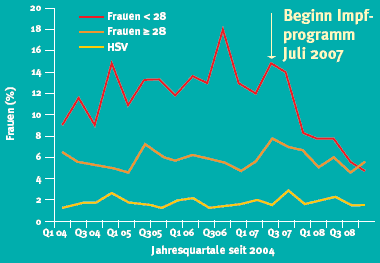
Wie effektiv die präventive HPV-Impfung in der Realität eingesetzt werden kann, hat das Beispiel Melbourne in Australien eindrücklich bewiesen. Im Rahmen eines nationalen Programms wurden ab 2007 bis zu 80% aller Mädchen in der Adoleszenz sowie junge Frauen im Sinne eines Nachholprogramms durchgeimpft. Bereits nach einem Jahr war ein früher Benefit durch die quadrivalente HPV-Impfung nachweisbar: Die Inzidenz neu aufgetretener genitaler Warzen sank bei den unter 28-jährigen Frauen hoch signifikant, währenddem sie bei den älteren Frauen gleich blieb (siehe Abbildung 4).
 |
|
Abbildung 4: Reduktion genitaler Warzen nach Einführung des Impfprogramms | |
| |
Keine Sicherheitsbedenken
Die Daten zur Verträglichkeit respektive Sicherheit der quadrivalenten HPV-Impfung in randomisierten Studien haben bei über 25'000 Frauen aus 33 Ländern keine Bedenken aufkommen lassen. Nebenwirkungen waren in den klinischen Untersuchungen bei über 17'000 Frauen zwischen 16 und 26 Jahren sowie in Langzeitbeobachtungen von über 51'000 Frauen selten. Inzwischen erhielten Frauen weltweit 50 Millionen Dosen und die Behörden in Europa und den USA haben die Sicherheit der Intervention aufgrund der Ergebnisse aus Pharmakovigilanz-Programmen bestätigt [19].
Während der Schwangerschaft wird eine HPV-Impfung nicht empfohlen. Trotzdem kann eine Exposition erfolgen, wenn die Schwangerschaft noch nicht bekannt ist. Im Gardasil Pregnancy Registry wurden 863 Frauen mit einer Impfung während einer Schwangerschaft erfasst. Die Raten spontaner Aborte, fetaler Todesfälle und kongenitaler Anomalien waren vergleichbar mit den Raten, welche bei Frauen ohne Impfung zu erwarten gewesen wären [20].
Seropositivität sagt nichts über den Impfschutz aus
Anogenitale Warzen und niedriggradige intraepitheliale Läsionen können vom Immunsystem der gesunden Frau durch die zellvermittelte Abwehr gegen frühe HPV-Antigene eliminiert werden. Die antikörpervermittelte Antwort auf die HPV-Infektion ist hingegen schwach und verläuft langsam. Eine Serokonversion innerhalb von 18 Monaten ist lediglich bei 54-69% der infizierten Frauen nachweisbar, wobei die erworbene Konzentration der Antikörper meist sehr niedrig ist. Wie hoch ein Antikörpertiter sein muss, um vor HPV-assoziierten Erkrankungen zu schützen, ist nicht bekannt. Sehr niedrige Konzentrationen scheinen eine hohe klinische Effektivität zu haben. Bei der Messung der Konzentration von Antikörpern ist zu bedenken, dass verschiedene Antikörper-Assays verschiedene Resultate liefern und diese untereinander nicht vergleichbar sind.
Die HPV-Impfung führt zu einer stärkeren humoralen Antwort als die natürliche Infektion. Der Hauptgrund dafür dürfte eine stärkere Exposition der Antigene im Blut und in den Lymphknoten nach intramuskulärer Injektion des Impfstoffs sein. Neutralisierende Epitope werden dem Immunsystem durch die Impfung in grösserer Anzahl angeboten und die Induktion der T-Helferzellantwort für B-Zellen ist stärker. Das ermöglicht eine potente Reaktion der Gedächtnis-B-Zellen und Immunantwort bei Infektion. Eine Korrelation zwischen Antikörpertiter und Effektivität oder Protektion vor HPV-Erkrankungen besteht nicht [21]. Die Seropositivität ist also kein guter Prädiktor für die klinische Effektivität; die Impfung gewährleistet gemäss bisheriger Erkenntnisse trotz sinkender Antikörperspiegel über die Jahre einen 100%igen Schutz [22].
Referenzen
1. International Agency for Research on Cancer (IARC), Globocan 2002
2. de Sanjosé S et al. Worldwide prevalence and genotype distribution of cervical human papillomavirus DNA in women with normal cytology: a meta-analysis. Lancet Infect Dis 2007;7:453-459
3. Bosch FX et al. Epidemiology and natural history of human papillomavirus infections and type-specific implications in cervical neoplasia. Vaccine 2008;26 Suppl 10:K1-16
4. Castle PE et al. A prospective study of age trends in cervical human papillomavirus acquisition and persistence in Guanacaste, Costa Rica. J Infect Dis 2005;191:1808-1816
5. Khan MJ et al. The elevated 10-year risk of cervical precancer and cancer in women with human papillomavirus (HPV) type 16 or 18 and the possible utility of type-specific HPV testing in clinical practice. J Natl Cancer Inst 2005;97:1072-1079
6. Insinga RP et al. The health and economic burden of genital warts in a set of private health plans in the United States. Clin Infect Dis 2003;36:1397-1403.
7. FUTURE II Study Group. Quadrivalent vaccine against human papillomavirus to prevent high-grade cervical lesions. N Engl J Med 2007;356:1915-1927
8. Saah A, for the FUTURE III Steering Committee. Efficacy of Gardasil against HPV 6/11/16/18 infection and disease in adult women. ESGO 2009, Abstract 1216
9. Rowhani-Rahbar A et al. Longer term efficacy of a prophylactic monovalent human papillomavirus type 16 vaccine. Vaccine 2009;27:5612-5619
10. Brown DR et al. The impact of quadrivalent human papillomavirus (HPV; types 6, 11, 16, and 18) L1 virus-like particle vaccine on infection and disease due to oncogenic nonvaccine HPV types in generally HPV-naive women aged 16-26 years. J Infect Dis 2009;199:926-935
11. Garland SM et al. Quadrivalent vaccine against human papillomavirus to prevent anogenital diseases. N Engl J Med 2007;356:1928-1943
12. Joura EA et al. Efficacy of a quadrivalent prophylactic human papillomavirus (types 6, 11, 16, and 18) L1 virus-like-particle vaccine against high-grade vulval and vaginal lesions: a combined analysis of three randomised clinical trials. Lancet 2007;369:1693-1702
13. Harper DM. Preliminary HPV vaccine results for women older than 25 years. Lancet 2009;373:1921-1922
14. Muñoz N et al. Safety, immunogenicity, and efficacy of quadrivalent human papillomavirus (types 6, 11, 16, 18) recombinant vaccine in women aged 24-45 years: a randomised, double-blind trial. Lancet 2009;373:1949-1957
15. Joura E et al. Impact of Gardasil® in women who have undergone definitive therapy. ESGO 2009, Abstract 366
16. Joura E et al. Short term Impact of Gardasil® in HPV-naive and HPV-exposed women Part I: CIN, VIN, VaIN and genital warts. ESGO 2009, Abstract 363
17. Joura E et al. Short term Impact of Gardasil® in HPV-naive and HPV-exposed women Part II: Pap tests, colposcopy, and definitive therapy. ESGO 2009, Abstract 365
18. Iversen OE et al. Overview of clinical trial efficacy results for the quadrivalent human Papillomavirus 6/11/16/18 vaccine Gardasil®, ESGO 2009, Abstract 388
19. Slade BA et al. Postlicensure safety surveillance for quadrivalent human papillomavirus recombinant vaccine. JAMA 2009;302:750-757
20. Sattler C et al. Overview of the post-marketing safety and effectiveness programms for Gardasil®. ESGO 2009, Abstract 376
21. Schiller JT, Lowy DR. Immunogenicity testing in human papillomavirus virus-like-particle vaccine trials. J Infect Dis 2009;200:166-171
22. Joura EA et al. HPV antibody levels and clinical efficacy following administration of a prophylactic quadrivalent HPV vaccine. Vaccine 2008;26:6844-6851
Mediscope
11.11.2009 - dde
Mit freundlicher Unterstützung von SPMSD